Нобелевская премия по химии в этом году была присуждена трем ученым, работающим в области дизайна и предсказания структуры белков. Половину премии получила Дэвид Бейкер в Вашингтонском университете в Сиэтле, США, а другая половина была присуждена Демис Хассабис и Джон Джампероба из Google DeepMind, базирующегося в Великобритании.
Почему структура белка достойна Нобелевской премии?
Мы давно знаем, что белки являются химическими инструментами жизни: существует множество различных типов белков, которые играют разные роли в нашем организме. Каждый белок состоит из цепочки аминокислот, которая складывается в определенную трехмерную форму или структуру, и функция каждого белка тесно связана с этой формой. Знание структуры белка помогает нам понять, как он работает, и на протяжении десятилетий ученые работали над способами выяснения белковых структур, что на этом пути создавало множество проблем.
В 1950-х годах развитие рентгеновской кристаллографии позволило исследователям получить первые трехмерные структуры белков. За эту работу Джон Кендрю и Макс Перуц были удостоены Нобелевской премии по химии в 1962 году.. С тех пор к набору инструментов были добавлены другие экспериментальные методы, такие как ЯМР и криоЭМ, и теперь исследователи определили структуры около 200 000 белков.
В 1972 году Американский биохимик Кристиан Анфинсен был удостоен Нобелевской премии по химии за открытие того, что именно последовательность аминокислот определяет способ сворачивания полипептидной цепи и что никакой дополнительной генетической информации не требуется. Это означает, что теоретически можно предсказать форму белка, просто зная его аминокислотную последовательность.
Это открытие привело к 50-летним поискам способа предсказать трехмерную структуру белка по его аминокислотной последовательности, но количество теоретически возможных конформаций белка, короче говоря, астрономическое.
Эта так называемая «проблема прогнозирования» стала величайшей проблемой биохимии и привела к запуску в 1994 году проекта, ставшего конкурирующим, под названием Критическая оценка прогнозирования структуры белка (CASP), целью которого было ускорить открытия в этой области. Однако прошло много лет, прежде чем был сделан значительный прорыв.
В этом году наградой были отмечены два разных открытия – почему они делят награду?
Работы этих трёх учёных тесно взаимосвязаны. Хассабис и Джампер использовали искусственный интеллект (ИИ), чтобы предсказать трехмерную структуру белка только на основе его последовательности. Тем временем Бейкер разработал вычислительные методы, которые могли бы решить обратную задачу: начать с белка с определенной структурой и выяснить, какую последовательность он будет иметь. Это позволило ему создать совершенно новые белки, которых ранее не существовало.
Вся эта работа основана на десятилетиях исследований и Нобелевских премиях по химии, направленных на понимание структуры белков.
Что на самом деле сделали лауреаты?
В 1990-х годах Бейкер начал исследовать, как сворачиваются белки. Используя эти идеи, он разработал Rosetta: компьютерное программное обеспечение для прогнозирования белковых структур.
Первоначально Rosetta использовалась для преобразования аминокислотных последовательностей в структуры, но после конкурса CASP 1998 года Бейкер и его команда решили использовать программное обеспечение наоборот; метод, который в конечном итоге привел их к созданию совершенно новых белков с нуля, также известный как дизайн de novo.
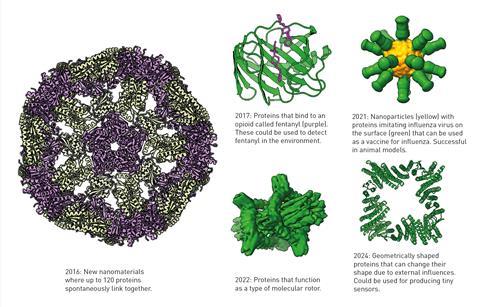
Для этого они нарисовали белок с совершенно новой структурой и попросили Розетту выяснить, какой тип аминокислотной последовательности приведет к образованию этого белка. Затем они ввели ген, кодирующий предложенную ими аминокислотную последовательность, в бактерии, которые произвели новый белок.Топ7. Используя рентгеновскую кристаллографию, они смогли определить, что созданный ими белок имеет структуру, очень близкую к той, которую они изначально разработали.
Работа Бейкера и его коллег была опубликовано в 2003 г. а код Rosetta был предоставлен мировому исследовательскому сообществу, чтобы обеспечить постоянную разработку программного обеспечения и новых приложений.
В 2010 году Хассабис, британский исследователь информатики и искусственного интеллекта, основал DeepMind Technologies. Первоначально DeepMind разработала модели искусственного интеллекта для популярных настольных игр, а после ее приобретения Google в 2014 году она достигла важной вехи в области машинного обучения, когда ее программа AlphaGo победила лучшего в мире игрока в го в 2016 году. Компания продолжила создание компьютерной программы на основе сверточная нейронная сеть – под названием AlphaFold.
В 2018 году AlphaFold опередила остальных на 13-м месте.й CASP конкурирует, достигая 60% точности предсказанных белковых структур. Но достижение более высокой точности стало новой проблемой.
Встречайте Джампера, исследователя с творческими идеями о том, как улучшить AlphaFold. Вместе Джампер и Хассабис совместно возглавили работу, которая привела к созданию AlphaFold2 в 2020 году, чему способствовали знания Джампера о белках и инновации, лежащие в основе огромного прорыва в области искусственного интеллекта — нейронных сетей, называемых трансформерами, — которые могли более гибко находить закономерности в огромных объемах данных, чем когда-либо прежде.
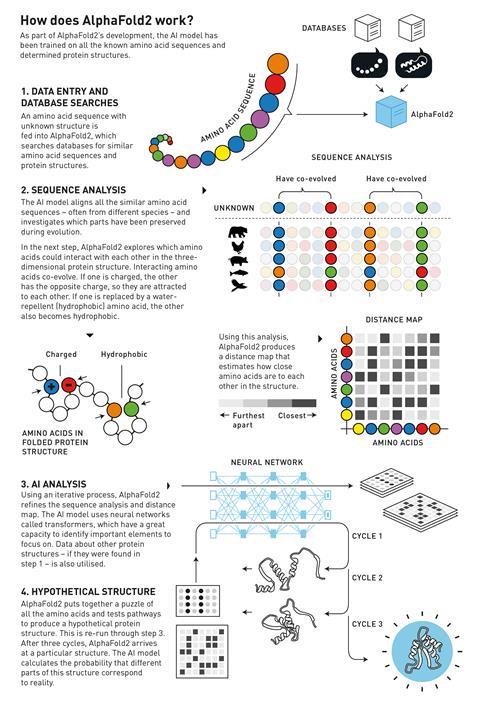
Когда в программу вводится аминокислотная последовательность с неизвестной структурой, она ищет в базе данных схожие аминокислотные последовательности и структуры белков. Затем сеть создает выравнивание сходных последовательностей, иногда принадлежащих разным видам, и ищет корреляции между ними, а также возможные взаимодействия между аминокислотами. На основе этой информации AlphaFold2 может затем итеративно уточнять карту расстояний, которая сообщает вам, насколько близки две аминокислоты друг к другу в пространстве, и анализировать последовательность. Наконец, он преобразует всю эту информацию в трехмерную структуру.
Сейчас AlphaFold имеет более 2 миллионов пользователей и позволил предсказать 200 миллионов белковых структур.
Каковы приложения этой работы?
Благодаря этим открытиям большинство мономерных белковых структур теперь можно предсказать с высокой точностью, и в результате были созданы большие базы данных, насчитывающие сотни миллионов структур. Белки являются настолько ключевым компонентом нашей биологии, что возможность их проектирования и прогнозирования их структуры открывает потенциальные возможности их применения в фармацевтике, наноматериалах и быстрой разработке вакцин, а также во многих других областях.
Означает ли это прекращение экспериментальных работ в этой области?
Нет сомнений в том, что разработка инструментов прогнозирования структуры белков искусственного интеллекта, таких как AlphaFold, представляет собой важную веху в структурной биологии. но они не заменяют экспериментальное определение структуры.. Экспериментально определенные структуры по-прежнему превосходят прогнозы, и они также будут необходимы для создания наборов обучающих данных для следующих поколений инструментов ИИ, а также для оценки эффективности этих инструментов при прогнозировании структур.
Одним из примеров постоянной необходимости в экспериментальных подходах является разработка лекарств. Хотя определение структуры белка может помочь сформировать идеи о том, какие соединения создавать дальше, существует множество других факторов, касающихся биологической активности белков, которые следует учитывать, таких как фармакокинетика, метаболизм и токсикология, которые в настоящее время не могут быть решены с помощью ИИ.
Гораздо более вероятно, что будущее структурной биологии будет за интеграцией высокопроизводительных экспериментальных исследований с ИИ, а не за его заменой.




.jpg)










